真空蒸餾的作用
真空蒸餾是利用被蒸餾物中各組分具有不同的揮發(fā)性能,對(duì)蒸餾物進(jìn)行低壓下加熱,通過(guò)控制蒸餾溫度使一些組分揮發(fā),而與另一些不揮發(fā)物達(dá)到分離進(jìn)行提純的目的。在鎂還原生產(chǎn)海綿鈦工藝中,對(duì)還原物進(jìn)行真空蒸餾的目的是除去海綿鈦中大部分MgCl2和鎂,工藝作業(yè)制度是一個(gè)溫度高(1000℃)、中真空和周期長(zhǎng)(120~200h)的過(guò)程。而真空自耗電弧熔煉這個(gè)真空蒸餾過(guò)程,與上述過(guò)程不同的是,工藝作業(yè)制度是溫度更高(1800℃)、中真空和周期較短(幾小時(shí)),它是前者的繼續(xù),可以除去海綿鈦中殘留的雜質(zhì),獲得純度更高的金屬鈦。
真空自耗電弧熔煉按反應(yīng)器的真空度,可以簡(jiǎn)化認(rèn)為蒸發(fā)的氣體流型屬于分子流。與普通蒸餾不同,分子蒸餾僅有被蒸餾物表面的自由蒸發(fā),沒(méi)有沸騰現(xiàn)象,從理論上說(shuō)這種自由蒸發(fā)是不可逆的。蒸發(fā)的氣體流型不同,其蒸餾分離系數(shù)α也不一樣。普通蒸餾分離系數(shù)為:![]() 分子蒸餾分離系數(shù)為:
分子蒸餾分離系數(shù)為:![]()
式中
Pi-i組元蒸氣壓;
Mi-i組元物質(zhì)的量;
ri-i組元活度。
鈦中各種雜質(zhì)按其與鈦的分子蒸餾分離系數(shù)相比,可以分成3種類型:第一種是am>1的雜質(zhì),這種雜質(zhì)可能分離,而且越大越易分離除去,特別是當(dāng)αm>100時(shí),雜質(zhì)較易分離除去;第二種是αm=1或接近1的雜質(zhì),這種雜質(zhì)無(wú)法除之;第三種是am<1時(shí)的雜質(zhì),這種雜質(zhì)在熔煉中無(wú)法除去,只能濃縮。
鈦和其他一些金屬雜質(zhì)的飽和蒸氣壓和溫度的關(guān)系見圖1-17和表1-3.一些雜質(zhì)對(duì)鈦的分離系數(shù)見表1-4.
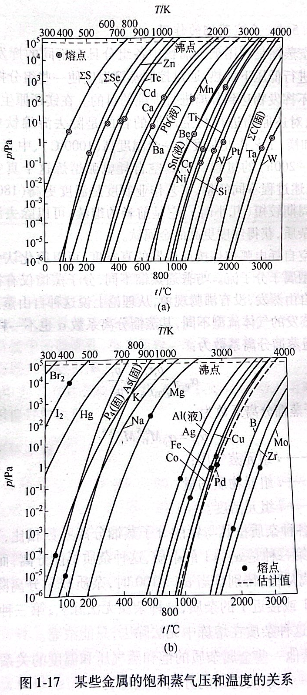
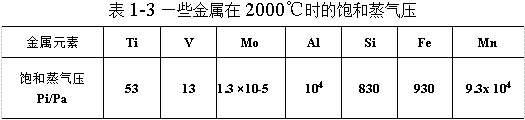
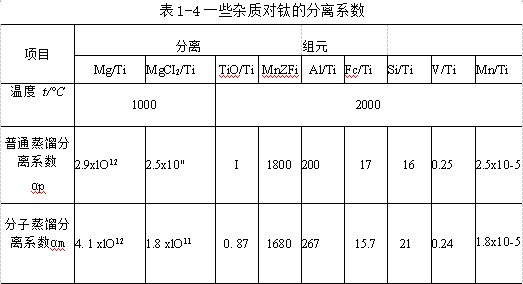
海綿鈦中屬第一類的游離雜質(zhì)是容易分離除去的。如Mg和MgCl2揮發(fā)性大,也大,500~600℃時(shí)開始揮發(fā),到達(dá)2000℃時(shí)基本上都能除去。又如吸附的水在更低的溫度下便開始揮發(fā)除去。
海綿鈦中夾雜的低價(jià)氯化鈦,如TiCl2和TiCl3,在一定溫度下發(fā)生離解反應(yīng):
2TiCl2-Ti+TiCl4
4TiCl3-Ti+3TiCl4
生成物中的氣態(tài)TiCl4被排出爐外。
海綿鈦中第二類間隙固溶體雜質(zhì)氧、氮和碳,它們不能以單元素解析排除,因?yàn)殁佄者@些氣體雜質(zhì)后無(wú)法解脫。可以認(rèn)為,它們?cè)阝佒幸遭伝颰iO、TiN、TiC形態(tài)存在。而這些鈦化物分解壓很低,很難離解。如TiN的分解壓在2331℃時(shí)只有0.31Pa(見表1-5).這些鈦化物只能以TiO、TiN和TiC 形態(tài)脫除。但是,它們和鈦的分離系數(shù)為1或接近1,如TiO/Ti的αp為1,無(wú)法通過(guò)熔煉脫除分離。

鈦中的TiO既不能加碳脫氧,也不能加氣體CO用還原的方法除氧。因?yàn)楦邷叵录犹蓟蚣覥O均會(huì)被鈦吸收或分解,相應(yīng)地會(huì)增加鈦中的雜質(zhì)碳和氧。
間隙性雜質(zhì)氫是唯一能解析脫除的。氫的解析也經(jīng)過(guò)一連串過(guò)程,先是氫原子向金屬界面擴(kuò)散,隨后在界面上結(jié)合成氫分子,氫分子最后在界面脫附,隨氣流排除。鈦含氫濃度低時(shí),生成物為TiH.TiH除氫時(shí),反應(yīng)歷程為:
TiH-Ti+H
2H-H2
氫化鈦的分解壓很大(見表1-6),其中的氫很容易被分解脫除。鈦錠的最終氫含量可以達(dá)到0.002%.
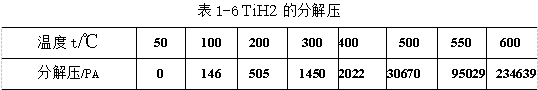
海綿鈦中第三類金屬雜質(zhì),和鈦分離系數(shù)am>1的有鐵、硅等,在熔煉中能揮發(fā)除去一些;和鈦分離系數(shù)am<1的有釩、鉬等低揮發(fā)性金屬,這類雜質(zhì)在熔煉中只能濃縮,但因含量甚微,不會(huì)引起明顯變化。
在上述易揮發(fā)組分中,H2O、H、TiCl2、TiCl和Ig 最易除去,而MgCl22的比較小且含量多,海綿鈦中Cl-含量約為0.05%~0.20%,可以認(rèn)為它是熔煉中要除去的關(guān)鍵組分,以此來(lái)分析除氣動(dòng)力學(xué)。
鈦真空自耗電弧熔煉時(shí),MgCl2等雜質(zhì)從液態(tài)鈦中的揮發(fā),由下述3個(gè)步驟組成:
(1)MgCl2從鈦液內(nèi)部通過(guò)邊界層遷移到熔池表面層;
(2)熔池表面層氣相MgCl2脫附和從表面揮發(fā);
(3)氣相MgCl2通過(guò)氣相界面層遷移到氣相內(nèi)部。
不同的雜質(zhì)元素或化合物的揮發(fā)脫除過(guò)程,因其揮發(fā)性不一樣而具有不同的控制步驟。蒸氣壓較小的雜質(zhì)Mo、V、TiO、TiN、TiC等,上述第二步驟為其蒸發(fā)脫除的控制步驟。蒸氣壓較大的雜質(zhì)Mg、MgCl2、H、Mn、Al等,上述第一步驟即邊界層傳質(zhì)速度是其蒸發(fā)脫除的限制性環(huán)節(jié)。
在真空條件下,第三步驟的速度很快,不會(huì)成為控制步驟,但在氬氣氛中熔煉時(shí)有可能成為控制步驟。
當(dāng)MgCl2的表面揮發(fā)速度(即第二步驟)成為控制步驟時(shí),有:
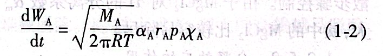
式中
dWA/dt-MgCl2的揮發(fā)速度;
αa-MgCl2的凝聚系數(shù);
PAp-純Mg的飽和蒸氣壓;
rA-MgCl2的活度系數(shù);
XA-MgCl2在碳中含量(摩爾分?jǐn)?shù));
M-MgCl2的物質(zhì)的量。
鈦中合金元素的揮發(fā)速度也同樣可以用式(1-2)進(jìn)行計(jì)算。當(dāng)控制步驟為第一步驟時(shí),出現(xiàn)表面MgCl2貧化現(xiàn)象,使之產(chǎn)生偏差,此時(shí)式(1-2)可寫成: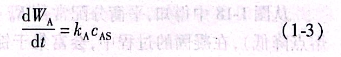
式中
Cas一熔池表面處MgCl2的濃度;
kA-氣相表面揮發(fā)系數(shù)。
液相邊界層的傳質(zhì)速度由下式表示:
dMA/dt=Kd(CA-CAs) (1-4)
式中
Ca-熔池內(nèi)部MgCl2的濃度;
Kd-液相邊界層傳質(zhì)系數(shù)。
達(dá)到穩(wěn)定時(shí)表面揮發(fā)速度和界面層傳質(zhì)速度相等,聯(lián)立式(1-3)和式((1-4),消去CAS值得到: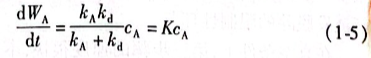
式(1-5)表明,不論揮發(fā)過(guò)程由氣相擴(kuò)散控制或由液相界面層擴(kuò)散控制,或者混合控制,揮發(fā)速度均和MgCl2濃度成正比,屬一級(jí)反應(yīng)。一般情況下,蒸氣壓大的MgCl2等雜質(zhì)的蒸發(fā)脫除屬擴(kuò)散步驟控制。由于Mgl2對(duì)Ti的分離系數(shù)am較大,擴(kuò)散速率也大,鈦中的MgCl2比較容易除盡。
億沐鑫新材料公司產(chǎn)品分類:鈦棒、鈦管、鈦板、鈦陽(yáng)極、鈦箔鈦帶、鈦法蘭、鈦絲、鈦靶材、鈦設(shè)備、鈦餅鈦環(huán)、鈦標(biāo)準(zhǔn)件、鈦加工件
 售前咨詢專員
售前咨詢專員
